[8 j1 N" T+ `2 e) I; ~' g: ~1 u3 S
( B4 n4 G3 f/ j, W. A4 }
# m5 C' y' ]' ^
【艾米丽的故事】2010年刚过完5岁生日的艾米丽(Emily Whitehead),不幸被诊断出急性淋巴细胞白血病,在进行首轮化疗时受到感染,差点失去双腿。后来病情复发,她又接受了治疗,并排期做骨髓移植手术。等待期间,病情再度复发,这时医生们已经无计可施。2012年艾米丽参与了一项史无前例的试验性疗法,接受Carl June博士的CART19细胞回输。她的体内发生了超强的免疫反应,大量免疫细胞“特种兵”正在剿杀她体内的癌细胞。连续几天发高烧,艾米丽不得不入院治疗。高烧下的她产生了幻觉,问爸爸:“我房间里怎么有池塘?”经历了噩梦般的连续高烧后,艾米丽最终挣脱了死神的束缚重新醒了过来。现在,Emily已经12岁,正在健康成长。她的体内仍然能检测到存活的CAR-T细胞。; w: u3 X9 i) y, O; k
" d5 ^: }+ O5 x( l2 ~& s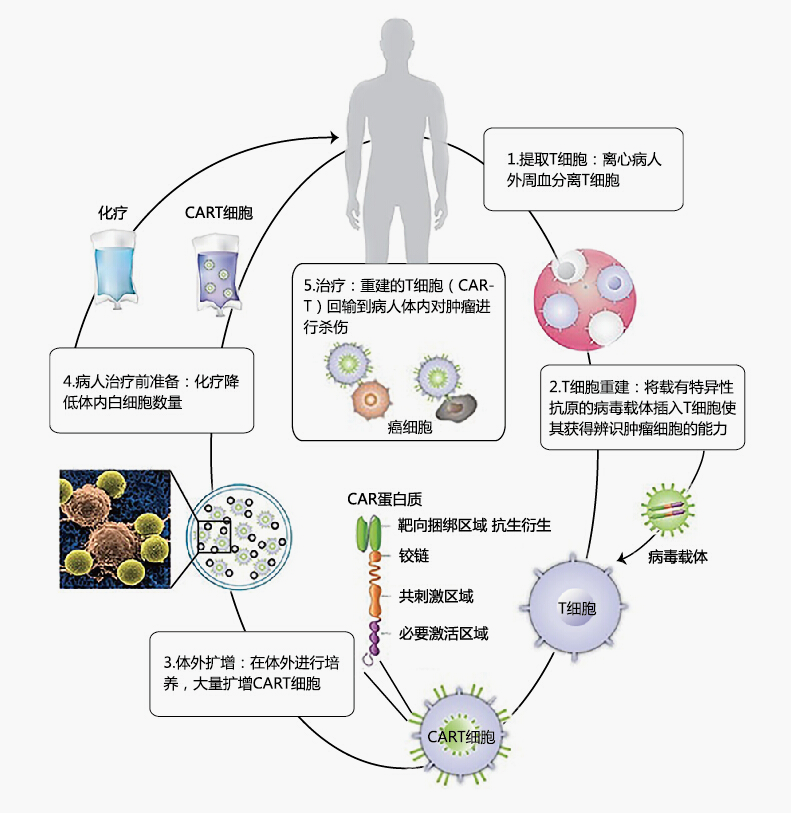
【CAR-T上市】近日,美国FDA批准首个CAR-T细胞产品CTL019,用于治疗25岁以下复发性或难治性B-细胞急性淋巴细胞白血病患者。CAR-T疗法(Chimeric Antigen Receptor T-Cell Immunotherapy),指的是嵌合抗原受体T细胞免疫疗法。CAR-T细胞疗法可以为每一个患者量身定制,基本程序是,1)分离:采集病人血液,分离血液成分提取免疫T细胞,2)修饰:通过对患者的T细胞(人体的一种免疫细胞)进行基因改造,使其可以杀死体内的癌细胞。3)扩增:体外培养,大量扩增CAR-T细胞。4.化疗:对病人进行小剂量化疗预处理,使免疫系统能留出一些空间。5)回输:把扩增好的CAR-T细胞回输到病人体内。 / Z3 ]7 Z$ @! h/ H7 h; d) k0 f- }
3 f$ [" C6 M8 T6 M/ L; c+ m1 B
8 j. q7 V+ a* p/ q2 y0 V+ ?" c
" S$ r% w% {; N! t2 a$ C* I6 J9 M3 J, ?+ x
【中状元】2017年8月31日,媒体宣称美国FDA已经批准诺华公司CD19CAR-T疗法Tisagenlecleucel上市,用于治疗难治性B细胞前体急性淋巴性白血病(ALL),商品名为Kymriah。成为美国第一个基因治疗产品,各种刷屏!打鸡血!!! 4 Y# n$ f0 F9 u! M
; J; B2 h, P9 Q5 y% i5 t" h 8 O/ e% Y+ C! |0 g7 p0 I& d' l 8 O/ e% Y+ C! |0 g7 p0 I& d' l
【西村老张问】隔壁老王买了小车(CAR-T),为啥邻里李大妈喜大普奔 $ D! ~: K* ]; ?/ U
! G/ V2 @% p2 k3 R; j, U/ J
3 U6 b! ]' ^6 j8 b% T7 Q# q4 j. w* L / V$ O7 _2 l5 H / V$ O7 _2 l5 H
【乌龙1:状元郎弄错了】紧接着,有人指出诺华的CAR-T并非美国FDA“第一个细胞治疗产品” 那么,到底谁是真正的状元郎? 6 u' T7 ~+ a! F/ y3 v2 Z
+ C3 K. O. r6 F) U1 O" t5 ~; J2 p, U
【状元1:今又生(重组人p53腺病毒注射液)】8 L7 Y+ U% X! r; s
2003年由中国药监局批准的全球第一个基因疗法药物,用于多种癌症的治疗。被誉为"是基因研究和生物高技术领域新的里程碑"。事实上,世界范围内至少有58个“重组人p53腺病毒注射液”在大大小小的制药公司中立项研究,但是它们全都倒在了漫长临床试验的路上。今又生被认为是一个时代早产儿,为争第一而“抢跑”并“弯道超车”的产物,上市后曾被质疑缺乏有足够的临床试验数据来确证其抗癌效果,也成为了CFDA永久的伤疤,至“今”也没“又生”。
- ^% \& i) c. }& ^0 f9 z* ~7 [- b
7 c1 J- j6 B5 c6 `! [/ U
& U2 A5 d* B% T4 j# H& q
【状元2:Provenge(Sipuleucel-T )】全球首个治疗性癌症疫苗,它由载有重组前列腺酸性磷酸酶(PAP)抗原的肿瘤患者自身的树突状细胞(免疫系统抗原的递呈细胞)构成。Provenge开发耗时近20年,2010年倍美国FDA上市,开创了癌症免疫治疗的新时代,它令罹患晚期前列腺癌的患者的平均存活时间延长了超过4个月。Provenge治疗一个病人开支为9.3万美元,疗法为一个月内三次注射。2015年原制造商Dendreon 公司宣告破产,2017年1月中国三胞公司以8.19亿美元接手Provenge。
9 Q' N3 _3 x( e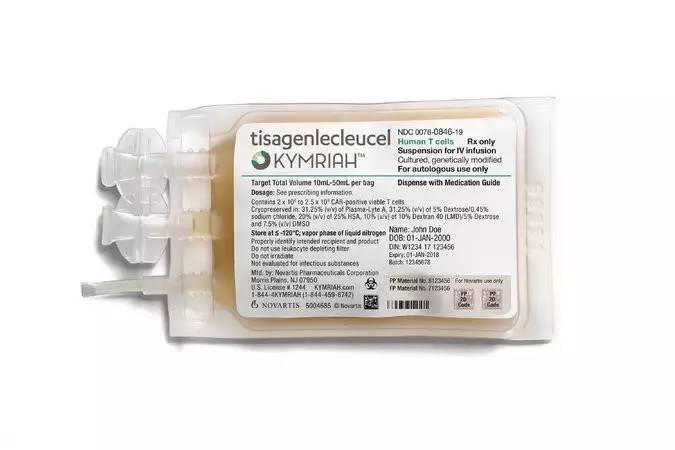 , `8 }5 Z/ a. r# M* c4 b K , `8 }5 Z/ a. r# M* c4 b K
; h( E. v3 j; v) O5 j3 o+ p; a5 s
【新科状元:Kymriah】的上市具有里程碑式的意义,CAR-T制备代表了细胞药物CMC的典范,Kymriah为个性化细胞药物杀开了一条血路,万里长征终于迈开第一步,值得生物医药领域同行的尊重与学习! * I+ J6 B8 C! J* o: n
. K5 t6 Q" g! H
9 H6 C! f! G% c3 q2 E$ _$ ?
8 b7 X+ [" |" w3 | z: k' m- ~【东村老刘问】隔壁老王的儿子中了状元,邻里李大妈激动个啥? ) U- U+ q1 l# O, h$ R! M
. Y( p% w! l7 q+ d4 K# S- j( W; J

: }) _. h% q M! ~1 z: R
9 M0 k) d6 F. t9 O! K
【乌龙2:用药剂量搞错了】中文媒体消息广为流传的Kymriah用法用量中,同样50kg上下体重细胞用量上限竟然相差50倍?不知哪个粗心大意的小编在50kg以上体重剂量总量上又加了“/kg”,使临床剂量在“1千万至2.5亿个T细胞”基础上又乘了50倍以上,原本CAR-T会引起强烈的“细胞因子风暴(CRS)和神经毒,如此这般疏忽会死人的! - G" J$ Y: Y! M

1 H d: q# [6 [1 Q. N1 j3 |
【Kymriah官方说明书中用药剂量】 8 @7 H$ i6 Y- N o
0 S( E2 G: p2 _
 ) J" L- E1 R& j6 O# i ) J" L- E1 R& j6 O# i
2 u1 v; \7 p5 t* }9 l, C b【CD19一扫光】Kymriah单支售价折合人民币320万元二成为“富人续命的选择”,未来能否实现盈利不禁要画上一个大大问号?同时,CD19 CAR-T输注后一年内半数白血病患者复发,并且会清除接受者的体液免疫体系,患者次序终生注射免疫球蛋白维持生命,更让人怀疑的接受者的生殖系统可能也遭到了摧毁,祈祷可爱的小姑嫩Emily将来不会怀上死胎或怪胎吧! ( M% U6 K7 r/ s
8 r9 @6 B2 @: |- x' D! s3 y1 f% Q 0 `& a2 o/ K" D' C 0 `& a2 o/ K" D' C
CMC (chemical manufacture control)——药物工艺质量开发 QbD (quality by design)——质量源于设计
【CAR-T一条街】! }& h, {! Z9 n; k% a, k
希望Kymriah一路走好,全球已经批准了十四个细胞药物,迄今只有韩国的Cartistem实现了盈利。虽然CFDA尚未受理任何CAR-T新药注册申请,从资本追逐盛况看,国内有朝一日或许会形成“CAR-T一条街”的壮丽景观,但愿不会有价无市。
/ N2 V& d2 S( S# t) }3 _
+ O8 r( J( i9 V4 `- y. i" q. }6 T. o4 K
|